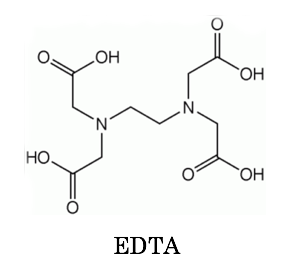
キレート滴定の実験で行った水の硬度の求め方について 大学でキレート滴定の実験を行ったんですが水の硬度がうまく計算できなくて教えていただきたいです 大学では アメリカ硬度=検液のモル濃度××1000 ドイツ硬度=検液のモル濃度×5608×1000×(100キレート滴定は、中和滴定などのようなイオン反応とは異なり反応が遅 いので、終点近くでは特に1 滴あるいは半滴ずつ滴下し、色の変化に注意 せよ。同様の滴定を3 回以上行う。 各実験台毎に各種滴定法で必要な器具・試薬を配布します。水の硬度測定 水の硬度とは、水に溶けているCa2+およびMg2+ の量をCaCO 3(ppm )に換算した ものである。硬度には、全硬度(Ca2+とMg2+),Ca硬度,およびMg硬度がある EDTA(エチレンジアミン四酢酸)は、最大6本の腕(6座配位)で2価~4価の金属イ
キレート滴定 Yakugaku Lab
キレート滴定 計算方法
キレート滴定 計算方法-4.キレート滴定 41 001Medta標準溶液の調製 要点 キレート滴定において標準溶液として用いられるedtaは、普通edtaの2ナトリウム 塩h2na2y・2h2oでetaと表示されている。この試薬は結晶水以外に多少の水分を含んでまで滴定する(ブロモクレゾールグリン試洷 2滴)。 アスピリンの定量 アスピリンの定量は,逆滴定に用いた硫酸について計算する。そのため,水酸化ナトリ ウムの量は計算には必要なく,操作中に溶け込んだ二酸化炭素は計算から除外される。



キレート滴定曲線 Androidアプリ Applion
京都大学 全学共通教育 基礎化学実験ホームページ:http//wwwchemzenkyohkyotouacjp/化学実験操作法:操作法 2 4 キレート滴定液名 01mol/L EDTA 電極名 自動入力先パラメータ 無し 滴定条件例 滴定曲線例 測定結果 測定回数 試料量(mL) 滴定値(mL) 濃度(g/L) 1 5 7623 9639 2 7603 9614 3 7622 9638 4 7611 9624 5 7595 9603 平均値 : 962g/L 統計計算 標準偏差 : 002g/Lキレート 滴定法で土壌中のカルシウム濃度が簡便に測定する ことが確認できたので,今後サンプル数を増やして データを取得していきたい。 3.結論 ①本実験では二酸化炭素を添加した水への炭酸カル シウムの溶解度が大きくなることがキレート滴定に
キレート滴定ではpH により試料と滴定試薬との反応性が変化するため、pH 調節は規定通り に行ってください。 光度センサーは純水で十分に洗浄後、水分を除去した状態で保管してください。 本体 : 電位差自動滴定装置(光度滴定用プリアンプリファイア PTA)実験問題2 キレート滴定とヨウ素還元滴定による 金属イオンの定量 (18 5 27, IChO50代表生徒強化訓練合宿@長崎大学) キレート滴定(錯滴定)とヨウ素還元滴定は,溶液中の金属イオンの定量方法として,代表的 な方法である。24ア ルミニウムのキレート滴定 キレート試薬を用いて、滴定法により金属イオンの定量を行う操作をキレート滴定と言う。 アルミニウムのキレート滴定では、キレート試薬としてエチレンジアミン四酢酸・ニナトリ ウム塩(edta・2na塩 と略す)を 使用する。
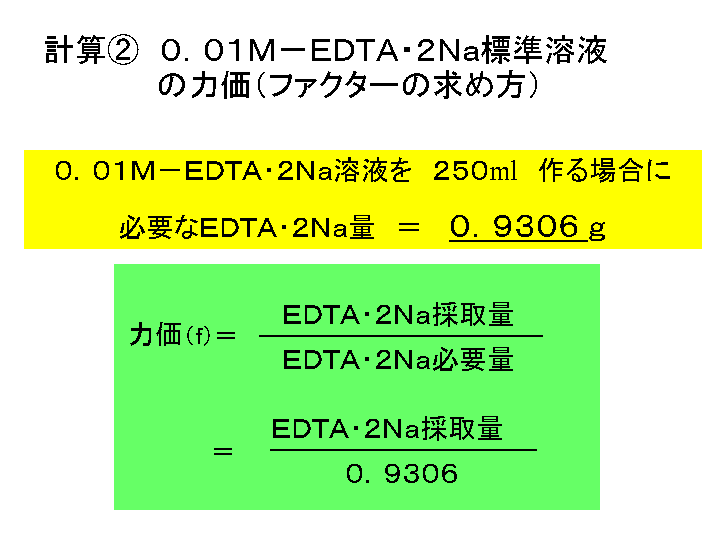
I 3 EDTA 2Na ① &Ø0 (j 001M xEDTA 2Na @A ˜ 150mL È e è / ② à EDTA 2Na @A < >˜ j'(p1 EDTA 2Na @A ˜ / ③ à S˜&j( CaCO 3 01 ˜˘ * / ④ k à S ˇˆ 2mL ˜ø‚Z ˙ > ˝"˛€˚˜W ˜pè $ HCl ˜Iî質問箱 名前: 芦田 実 日時:02年09月22日 14時50分 岸本 博文 様 必ずしも専門家ではありませんので,不正確な回答もあります.教育学部から公開しているホームページの質問箱とQ&A集にも回答(一部)を載せたいと思います. 質問18 キレート滴定法キレート滴定の計算方法 1 試薬の体積と初濃度 塩化アンモニウムNH 4 Cl-アンモニア水NH 3 系のpH緩衝液により,常にpH=10一定であると仮定する.計算を簡単化するために,カルシウムイオンCa 2 やマグネシウムイオンMg 2 と指示薬のエリオクロムブラックT(EBT)の錯体形成反応(化学平




キレート滴定14




比色試薬 金属指示薬 Xo 同仁化学研究所
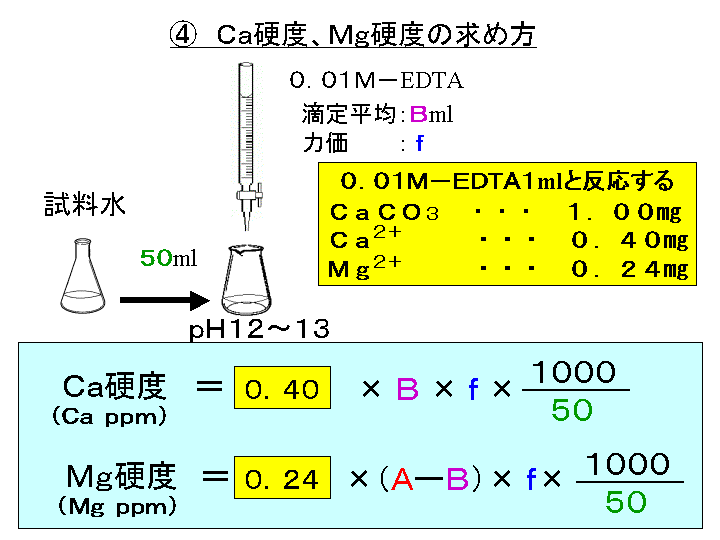
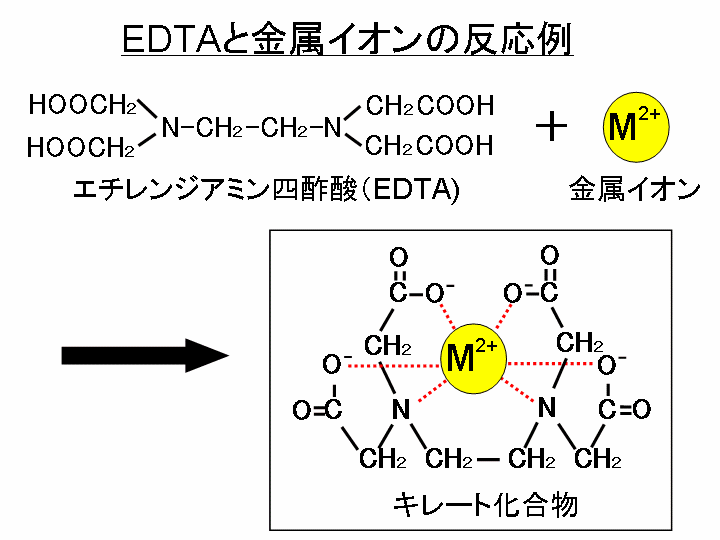
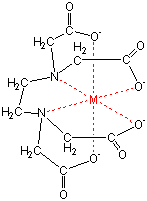
3.edtaによるキレート滴定 競技では,edtaによるキレート滴定の原理やebt指示薬やnn指示薬を用いてca2+ やmg2+ を定量する具体的な方法を問題文の1,2ページに記載し,初学者にも充分理解で きるように配慮した。次に実験操作の手順を簡潔に示す。ビュレットの0.01M-EDTA標準溶液で滴定を行う。 溶液の色が赤紫色から青色になったところを終点とする。 6) 1~5を3回繰り返し、滴定平均値を求める。 7) Ca硬度を計算し求める。 8) Mg硬度を計算し求める。滴定用キレート試薬として、ドータイト2na(edta2ナトリウム 塩)、その他ドータイト金属指示薬、キレート滴定用補助試薬など、 キレート滴定に必要な試薬類は全部とりそろえているので、ご利 用いただきたい。 nc h2ch2 n ch 2cooh hoocch2 ch2cooh hooc 2 on o n m ch2 ch2



水の硬度測定 キレート滴定




キレート滴定法 上野景平 著 池袋ブックサービス 古本 中古本 古書籍の通販は 日本の古本屋 日本の古本屋
計算式は次のようになります。 滴定曲線例 測定結果 滴定条件例 測定回数 試料量 滴定値 全ニッケル濃度 (mL) (mL) (g/L) 1 1 2 1 3 1 170 平均値 : 1124 g/L 統計計算 標準偏差 : 0376 g/L 変動係数 : 033 %ト滴定法は,エ チレンジアミン四酢酸 (EDTA)及びその類縁体が,多くの金属イオン と価数に依らず1:1のキレート錯体 を形成することを利用した金属イオンの容量分析法である。この方法は,主にCa2 +及びMg2+の滴定法(水の硬度の測定)として知水の硬度測定 1 はじめに 硬度 1) とは,水に含まれるCa 2 とMg 2 の量を表す指標であり,この値に基づいて軟水や硬水 2) といった水の硬さが決められている。 軟水は口当たりがまろやか,硬水は苦みのような口当たりといわれている。近年,スーパーなどで多くの種類のミネラルウォーターを



2



水の硬度測定 キレート滴定
キレート滴定法は,金属キレート錯体の生成反応を利用して,金属イオン を定量する方法である。たとえば,水道水など飲料水中に含まれるマグネシ ウムおよびカルシウムイオン濃度,すなわち,水の硬度はedta を用いる キレート滴定によって簡単に測定キレート滴定 1.目的 キレート滴定法を用いて、未知試料中に含まれる金属イオン(Ca 2+、Mg 2+)の濃度 を調べ、さらに水の硬度についても計算して求める。また、実験を通してキレート滴定法 の原理や操作の仕方について学び、結果の考察をしてさらに理解を深める。‒ 133 ‒ キレート滴定シミュレーションのインターネットによる自動サービス 芦 田 実 埼玉大学教育学部理科教育講座 村 田 龍 一 株式会社ワクシス・エンタープライズ 長 岡 淳 子 首都大学東京大学院社会科学研究科 キーワード:定量分析、キレート滴定、濃度計算、遠隔支援



キレート滴定の原理とエチレンジアミン四酢酸 Edta の性質についてわかりやすく解説 ジグザグ科学 Com



水の分析
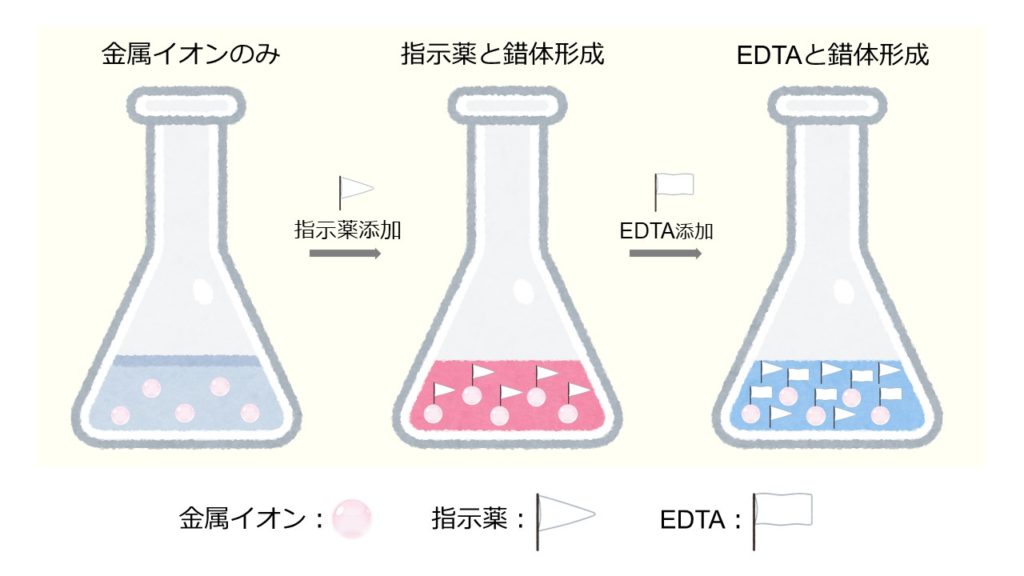
示薬としてedta溶液で滴定し,edta溶液の正確な濃度を決定する。 4.キレート滴定によるca2+とmg2+の定量 試料水にph 10緩衝液を加え,edta溶液とebt指示薬を用いてキレート滴定を 行い,試料水に含まれるca2+とmg2+の合計量を定量する。キレート滴定の基礎(Ⅰ) キレート滴定の基礎(Ⅰ) 天 満 照 郎※ 1 はしがき キレート滴定法が創始されてから 年,多くの金属の 定量に利用され,その有用性は増大の一途をたどってい る。edta のような優れたキレート化剤が安価に入手でNn指示薬 キレート滴定の指示薬(錯形成→ 赤:遊離→ 青) edta溶液 滴定剤 有機廃液タンクへ (注ぎ口にろ紙をつけておくこと!) 実験の注意事項 edta滴下 (1) 『ホールピペットで取る』と指定が無いものは大体でok!
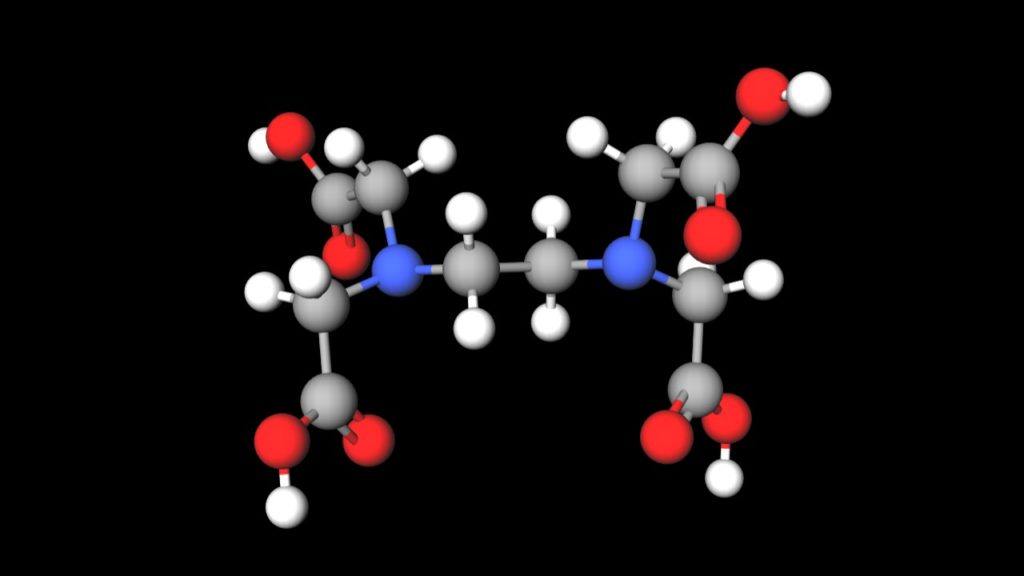



キレート滴定の原理とエチレンジアミン四酢酸 Edta の性質についてわかりやすく解説 ジグザグ科学 Com



2
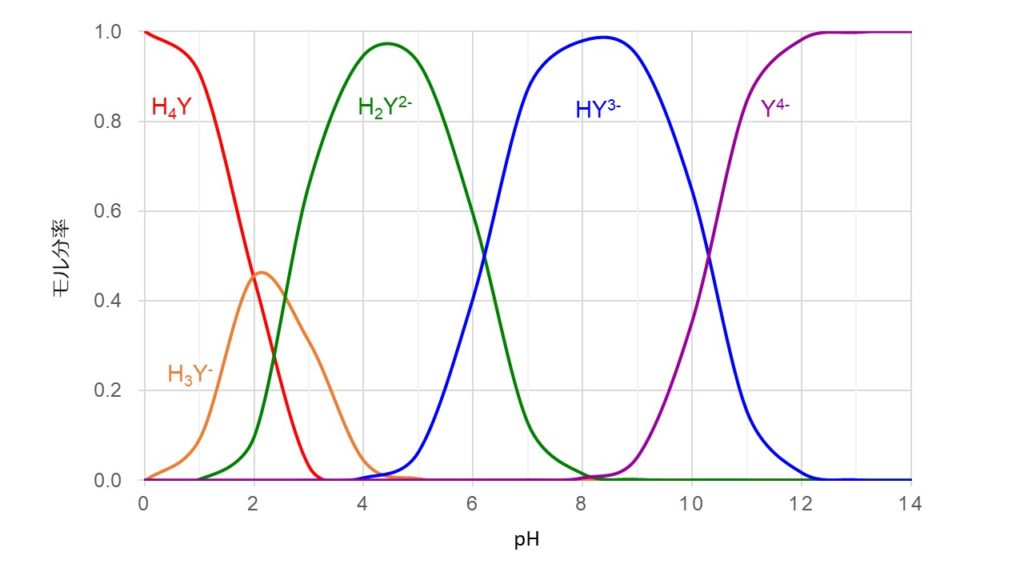
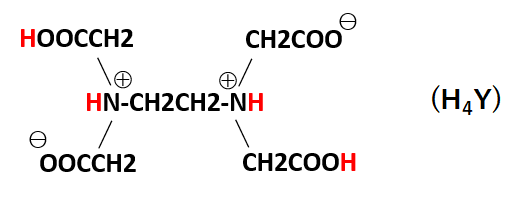
(2)容量分析(キレート滴定,酸化還元滴定,中和滴定,沈殿滴定)を実験できる。 (3)報告書(レポート)の作成方法を実践できる。 第2学年 物質工学科 履修 2単位 必修 実験 到達目標 ② 容量分析のキレート滴定・ 酸化還元滴定・中和滴定・ 沈殿滴定の類似点と 放置し,その 210g をとる。 別に,炭酸ナトリウムをあらかじめ白金るつぼに入れ,600℃で加熱し て恒量とし,その 265g をとる。 両者を少量の炭酸を含まない水 2 (12) (b) によるに溶かし,全量 24 K 0101 1998 フラスコ 1 000ml に移し入れ,さきの炭酸をキレート滴定 エチレンジアミン四酢酸(edta、h 4 yと略記)は、水溶液中で金属イオンと反応し、 非常に安定な金属キレート化合物を作る。 キレート滴定は、そのことを利用した容量分析法である。キレート生成反応は、 である。



2



キレート わかりやすく
化学実験(キレート滴定)での考察の書き方が分かりません。※実験で全硬度とCa硬度とMg硬度を求めます。 四塩基酸のH4EDTA 薬剤師・薬学生のメモ帳 問242~回薬剤師国家 JSTAGE Home 輸液処方設計の基礎知識* 硬度の計算方法を教えてください。1.目的 2.原理 3.操作方法 4.結果 5.濃度計算 6.課題(x線構\造回析法、edtaキレートはどのような構\造の化合物か?方法が広く用いられている。これをキレート滴定という(参考(1)参照)。ここでは水の硬度測定すなわちCa2,Mg2の濃度を キレート滴定によって定量する方法を理解する2)。 < 要 点 > 硬度とは水中のCa2およびMg2の量をCaCO 3(mg CaCO3/L)に換算したものである




キレート滴定
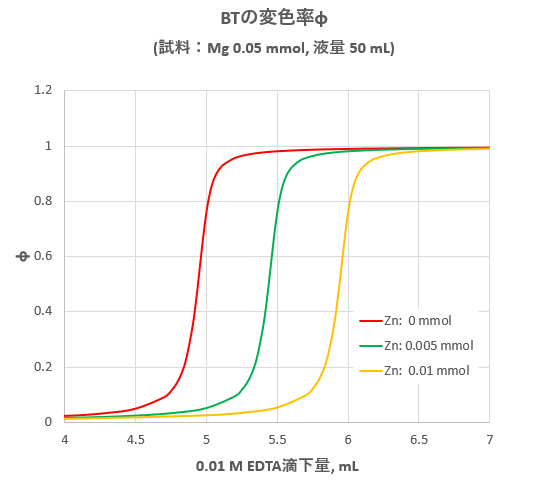



Edta滴定における妨害金属イオンのマスキング 滴定曲線 溶解度などーエクセルを用いて
33.キレート滴定 キレート滴定では、金属イオンとキレート試薬(もっぱらedtaが使われる)が安定な錯体を作ることを利用する。 したがって、たとえば ebt の場合は滴定の終点として、完全に赤みの消えたところを取る。キレート滴定法の原理で,こ の方法により,2価 以上の 金属イオンのほとんど全部がedtaに よって滴定でき るようになりました それで問題はどのような方法で遊離金属イオンのなくNhk高校講座 化学基礎 第32回 中和滴定 nhk高校講座 反応に要する2つの水溶液の体積を正確に測定すれば、濃度を計算で求めることができるんだ



年11月発行 カルシウム塩のキレート滴定について
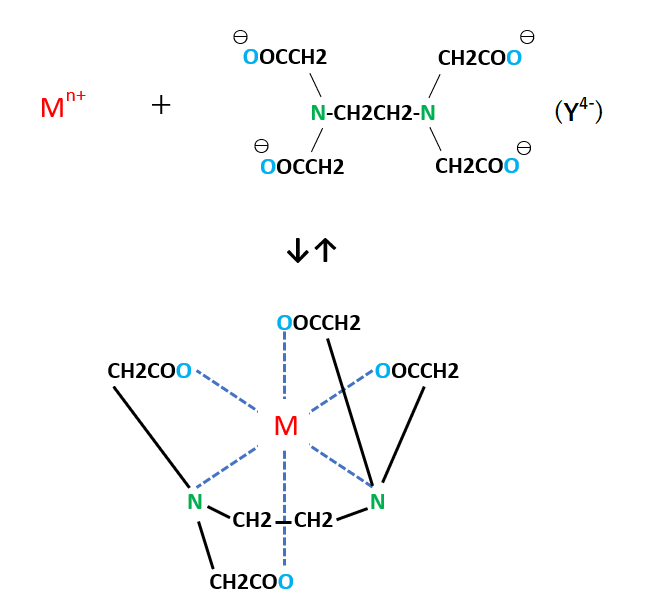



Edta滴定の基礎 滴定曲線 溶解度などーエクセルを用いて
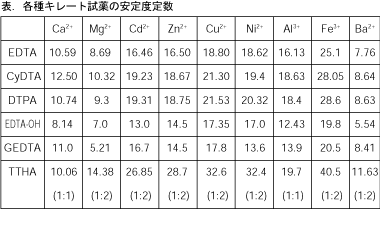
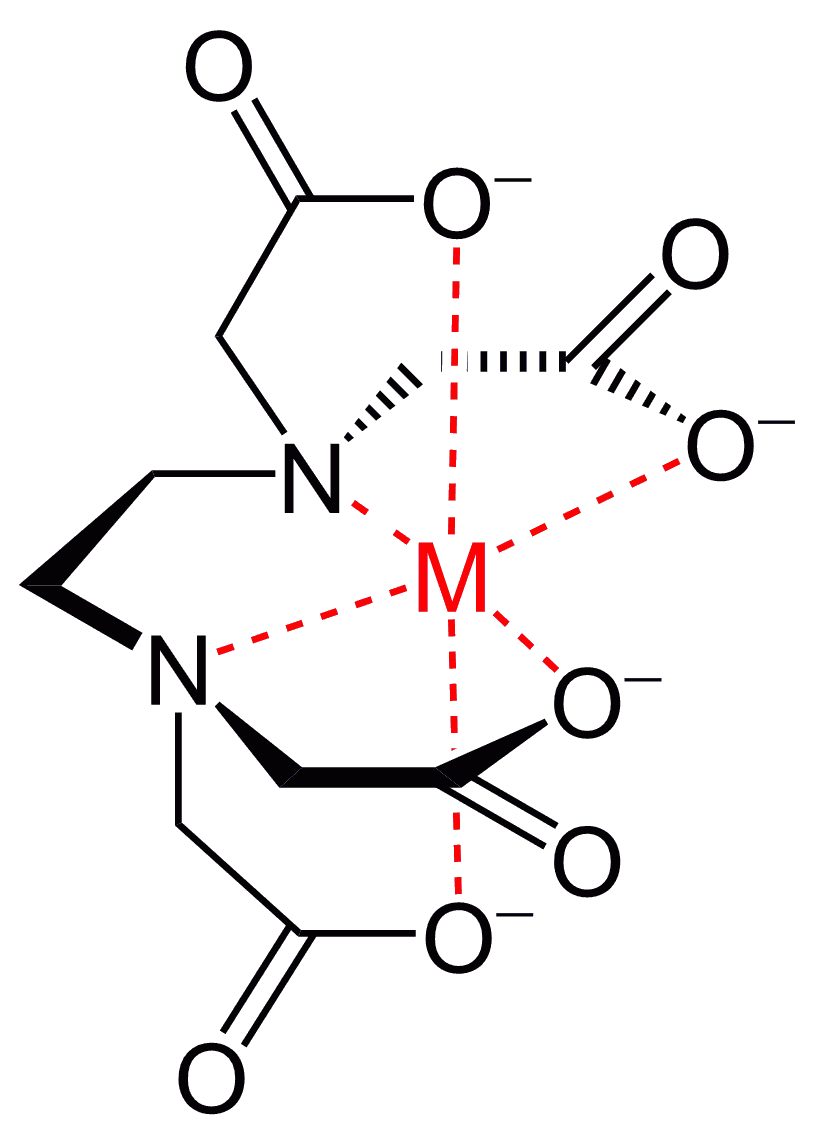
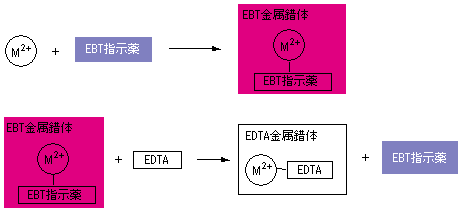
144 XIII5 標準液の調製と標定 (1)005mol/L エチレンジアミン四酢酸二水素二ナトリウム液 C10 H14 N2Na 2O8・2H 2O()g/L 調製 EDTA ・Na 2 19g を水に溶かして 1000mL とする。 ポリエチレン瓶に保存す水の硬度とは、水に溶けているCa 2+ およびMg 2+ の量をCaCO 3 (ppm)に換算したものである。 硬度には、全硬度(Ca 2+ とMg 2+ )、Ca硬度、およびMg硬度がある。 EDTA(エチレンジアミン四酢酸)は、最大6本の腕(6座配位)で2価~4価の金属イオンと、そのイオンの価数に関係なく1:1で結合しキレート滴定キレートテキテイchelatometric titration キレートメトリー (chelatometry),コンプレクソンメトリーともいう.水溶液中で金属イオンとキレート試薬との キレート 生成反応を利用して行う定量分析法で,終点の決定には 金属指示薬 ,pH変化の測定




京都大学 化学実験操作法 操作法 2 4 キレート滴定 Mg イオンの定量 Youtube




土 日開講 分析化学応用学科 実験を繰り返して プロになる せんせのブログ 日本分析化学専門学校
水の硬度計算 こんなサイトがあるとは知りませんでした。 ありがとうございます。 馬鹿なことをお伺いしますが、ペットボトルには100mL中の成分表示がされています。 これをそのまま入力すればよいのですよね。 入力欄は1L = 1000mL辺りの含有量になり キレート滴定法のほか、icp 発光分光分析法も硬度の測定方法の一つです。icp 発光分光分析法は、プラズマ に導き入れた試料中のカルシウム等が発する光を測定して、その濃度を求める方法です。ではプラズマとは何で しょうか。
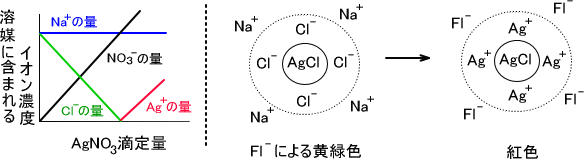



重量分析 定量分析




書籍紹介 分析化学の基礎 木村 優 中島理一郎 共著 化学




硬度1500mg Lのかた い水がある 水の硬度測定 バイオ科 応用バイオ化学実験 分析化学 2年 036 ブログ 学校のいまを知る 専門学校 東京テクニカルカレッジ




キレート滴定 Yakugaku Lab




キレート滴定



硬度の計算方法を教えてください 水1l中にcaが16mg Mgが Yahoo 知恵袋
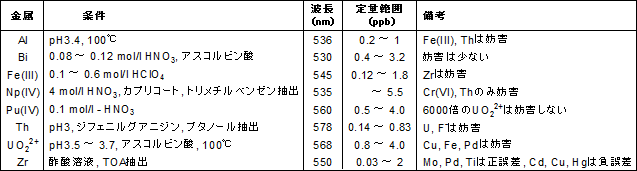



比色試薬 金属指示薬 Xo 同仁化学研究所




滴定計算 滴定についてよくある質問 定義 モル濃度方程式 曲 Lorett




キレート滴定法 上野景平 著 池袋ブックサービス 古本 中古本 古書籍の通販は 日本の古本屋 日本の古本屋
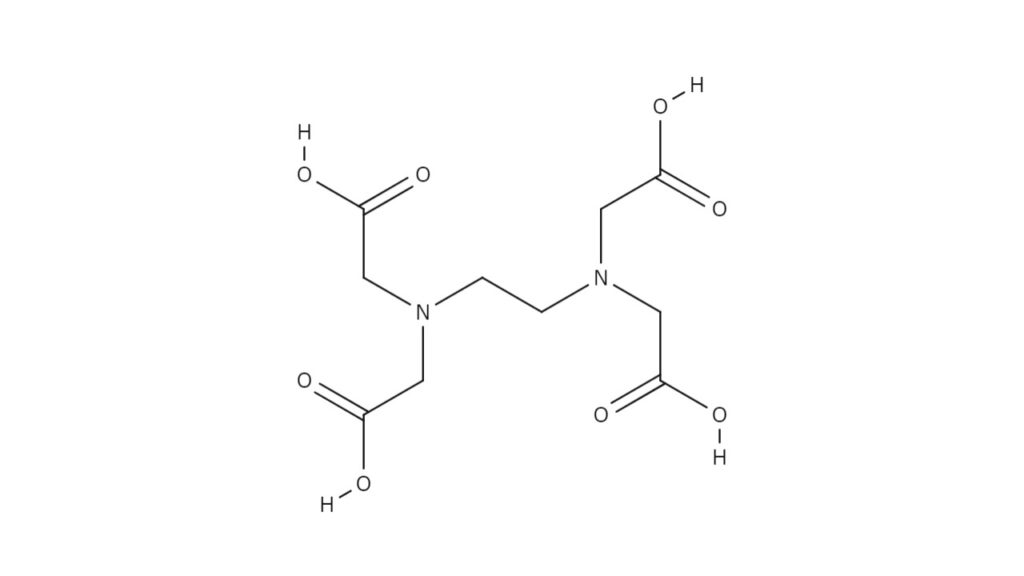



キレート滴定の原理とエチレンジアミン四酢酸 Edta の性質についてわかりやすく解説 ジグザグ科学 Com
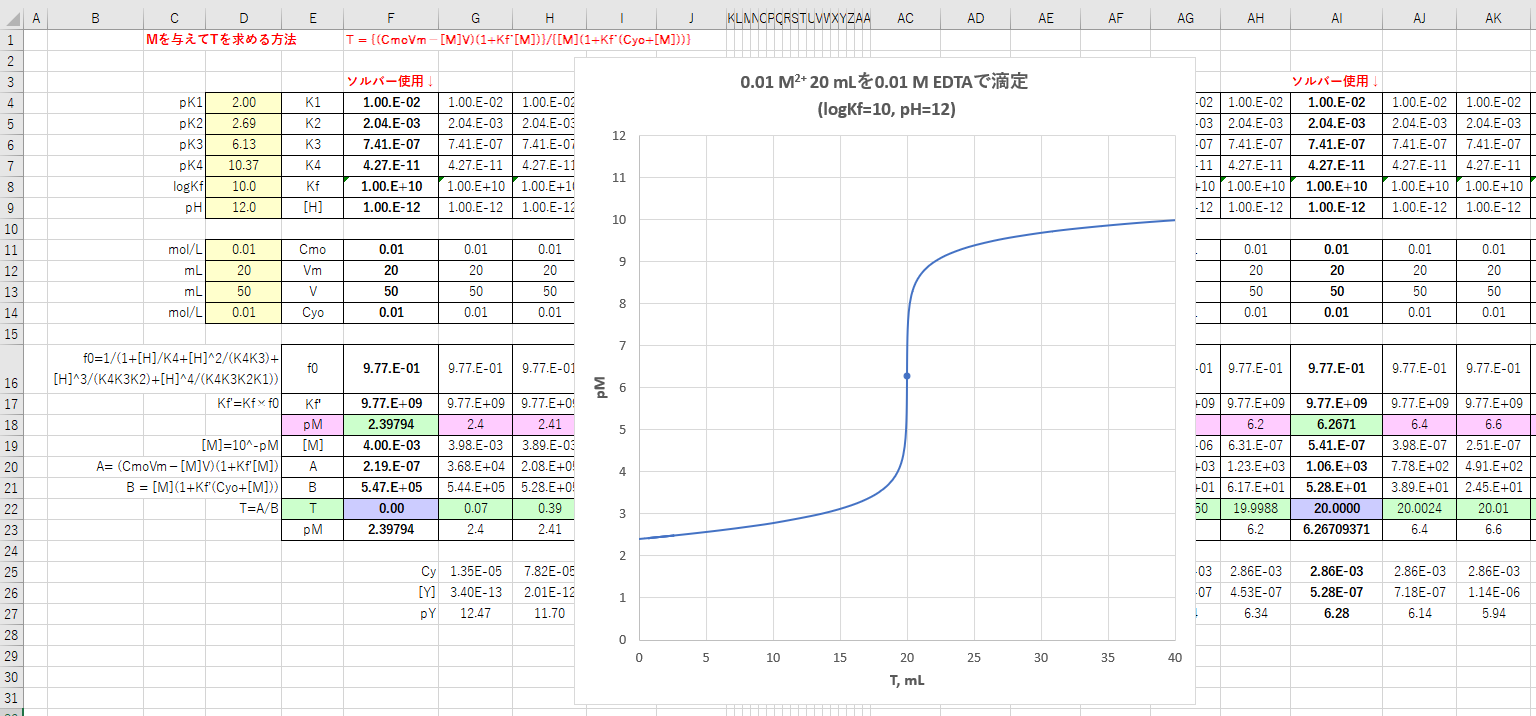



Edta滴定の基礎 滴定曲線 溶解度などーエクセルを用いて




キレート滴定の原理とエチレンジアミン四酢酸 Edta の性質についてわかりやすく解説 ジグザグ科学 Com
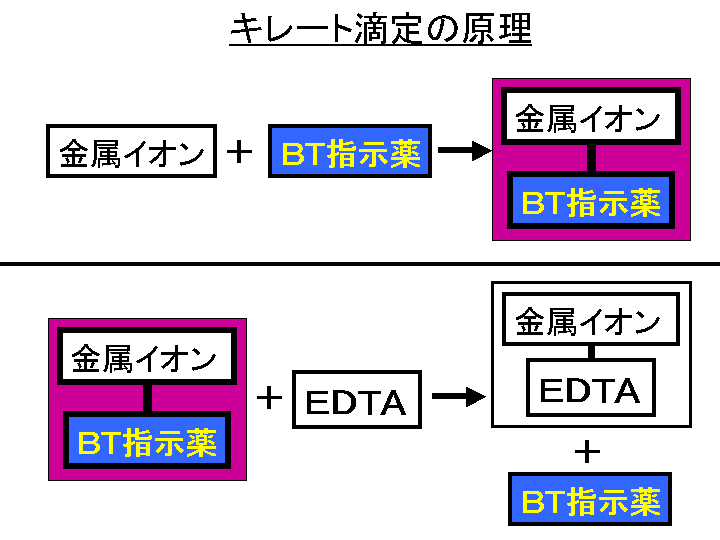



水の硬度測定 キレート滴定




キレート滴定



1



Column



比色試薬 金属指示薬 Pan 同仁化学研究所



キレート滴定曲線 Androidアプリ Applion



マイクロスケール化 今までビュレットを用い キレート滴定法で硬度を判断していた 今回は ビュレットを用いず簡易的に硬度を測定する方法を開発し マイクロスケール化をすることで 子ども達にも安易に実験ができるようにする 準備物 材料



キレート滴定 Yakugaku Lab



キレート滴定の濃度計算問題についてです 解き方がわからないので 教えていただ Yahoo 知恵袋



キレート Wikipedia




17 号 キレート剤の定量方法 Astamuse




キレート滴定 Yakugaku Lab
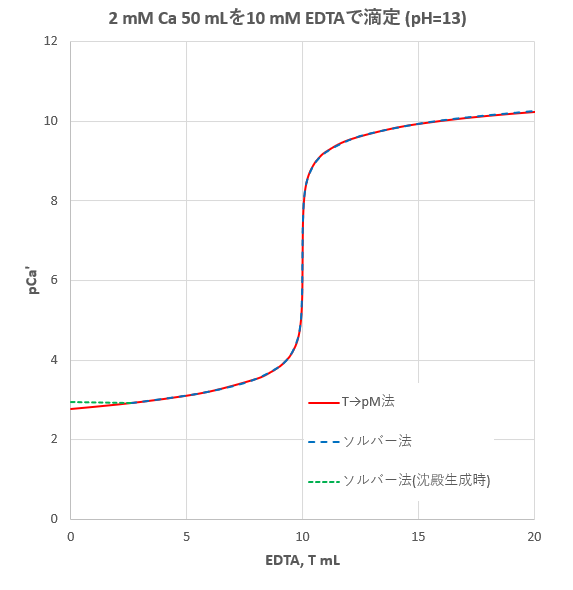



カルシウムのedta滴定 2 滴定曲線 溶解度などーエクセルを用いて
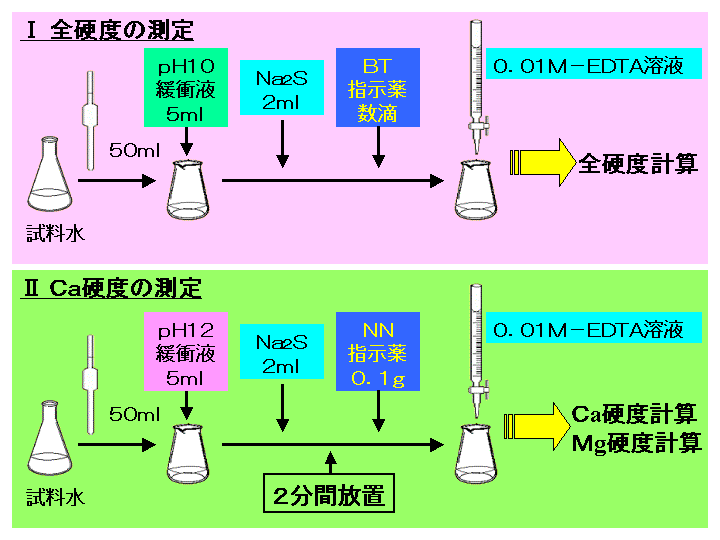



水の硬度測定 キレート滴定
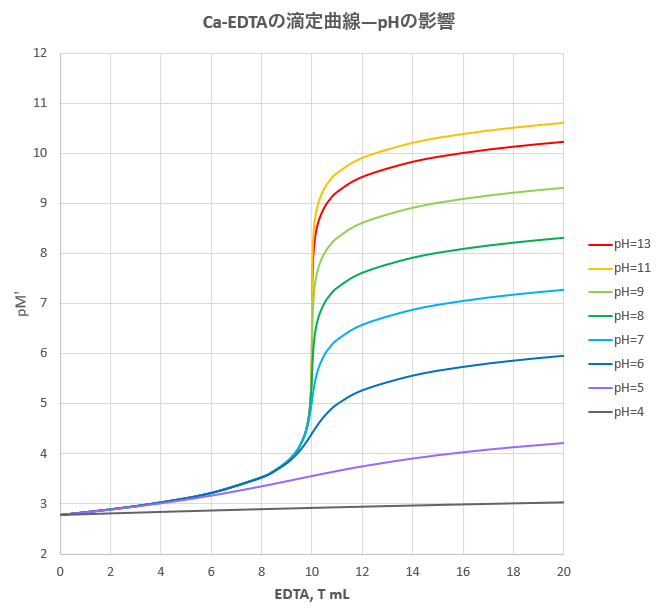



年05月 滴定曲線 溶解度などーエクセルを用いて
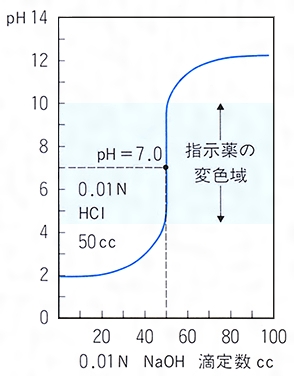



滴定とは コトバンク



水の硬度 株式会社ユニケミー ユニラボ




比色試薬 金属指示薬 Pan 同仁化学研究所




1999 1017号 滴定制御方法 Astamuse



2



2




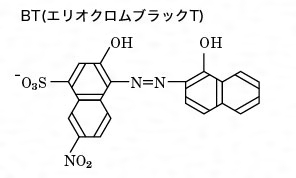
比色試薬 金属指示薬 Bt 同仁化学研究所



2




水の硬度測定 キレート滴定



水の硬度測定




灰中の酸化カルシウム



2



水の硬度 株式会社ユニケミー ユニラボ
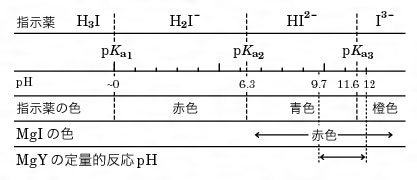



キレート滴定とは コトバンク



質問箱



水の硬度測定 キレート滴定



2
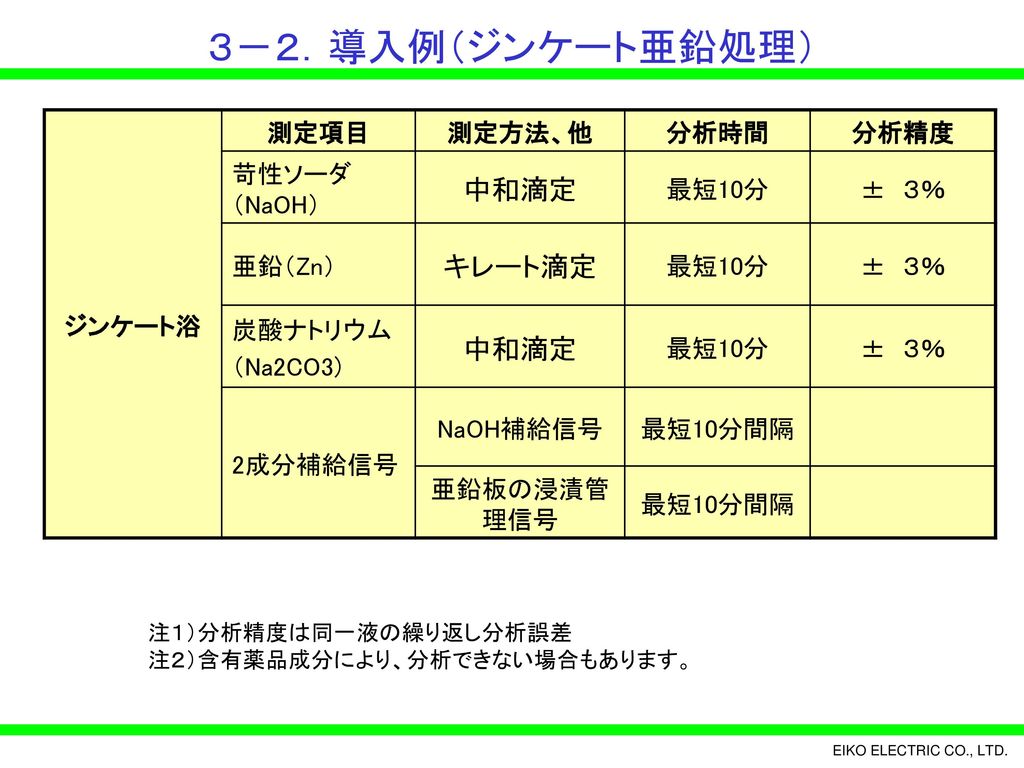



薬液処理浴自動管理装置 めっき管理主任シリーズ のご紹介 Ppt Download



2



Ibaraki Ct Ac Jp




キレート滴定 薬学 これでok




容量分析法 キレート滴定 問題解説 Youtube



2



キレート滴定の問題です よろしくお願いします Yahoo 知恵袋




水の硬度測定



化学キレート滴定の問題です 赤線引いたところの意味がわかりません Yahoo 知恵袋



キレート滴定とは コトバンク




17 号 キレート剤の定量方法 Astamuse




17 号 キレート剤の定量方法 Astamuse



1



水の硬度測定




水道水と飲料水の硬度測定 硬度 キレート滴定 マスキング剤 Transblog
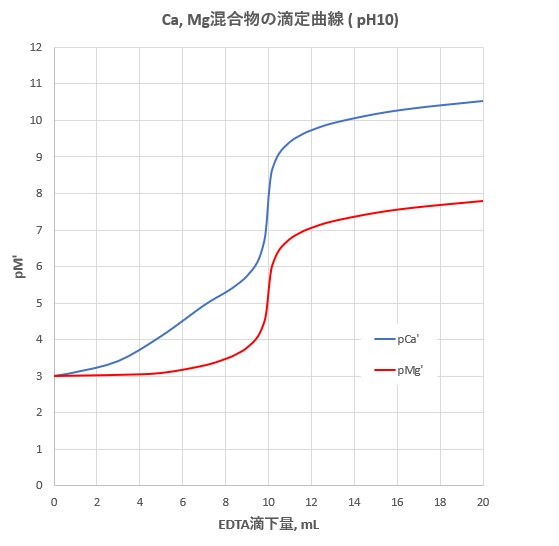



Edta滴定によるcaおよびmgの分別定量 滴定曲線 溶解度などーエクセルを用いて
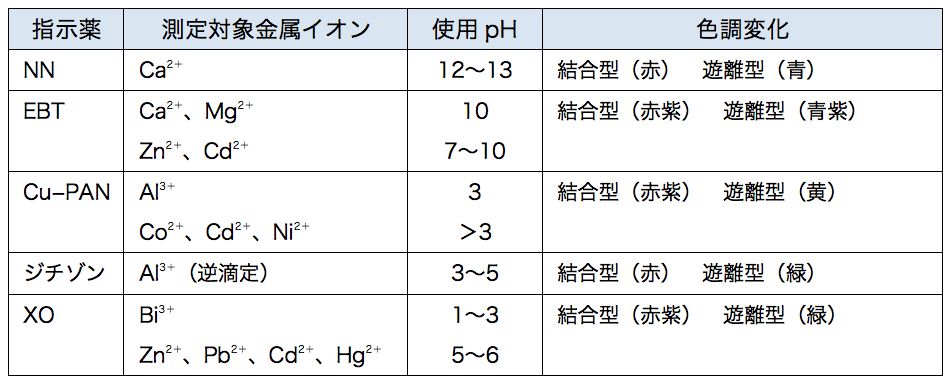



キレート滴定 Yakugaku Lab




エチレンジアミン四酢酸 Edta 化学徒の備忘録




分析実務たん 紫杏 数式を書くのが面倒なので手書きで




水の硬度測定




安定度定数とは コトバンク



キレート滴定の原理とエチレンジアミン四酢酸 Edta の性質についてわかりやすく解説 ジグザグ科学 Com



2




キレート滴定法の意味 用法を知る Astamuse
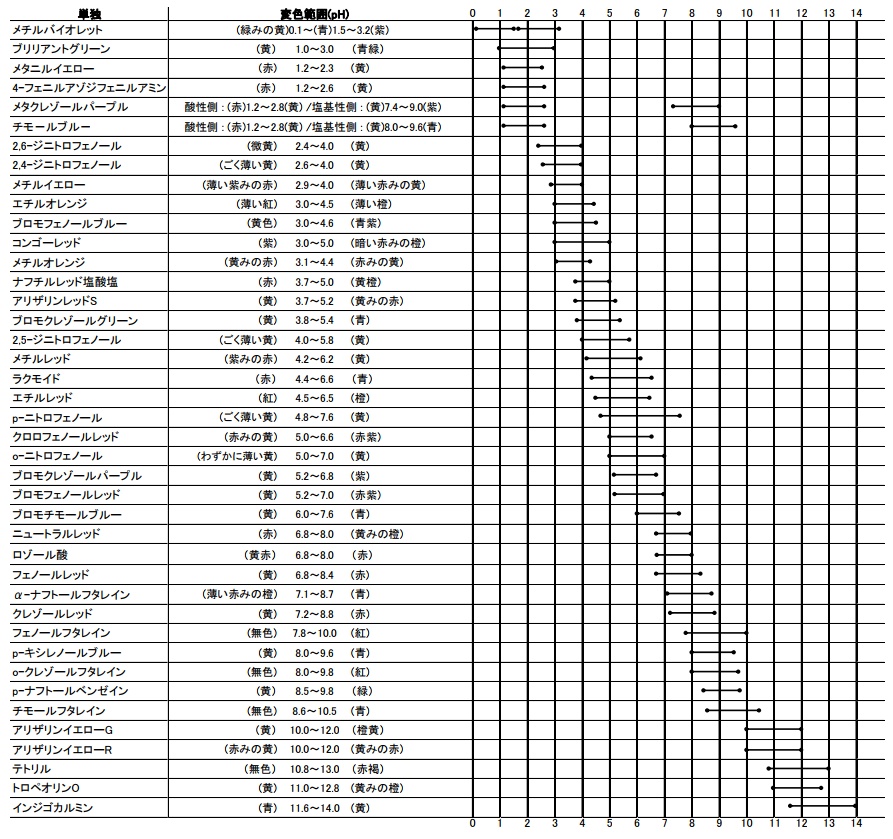



Ph指示薬変色範囲 お問合せ 試薬 富士フイルム和光純薬
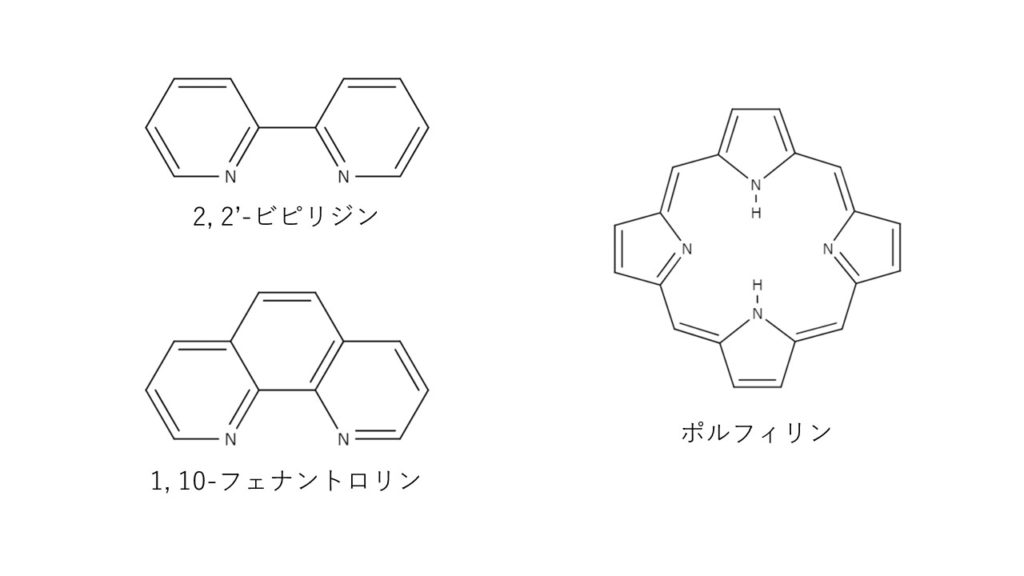



キレート滴定の原理とエチレンジアミン四酢酸 Edta の性質についてわかりやすく解説 ジグザグ科学 Com




滴定計算 滴定についてよくある質問 定義 モル濃度方程式 曲 Lorett



Edta滴定の基礎 滴定曲線 溶解度などーエクセルを用いて
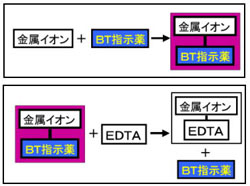



水の硬度測定 キレート滴定




17 号 キレート剤の定量方法 Astamuse




キレート滴定




エチレンジアミン四酢酸 Edta 化学徒の備忘録



Www2 Ube K Ac Jp




水道水と飲料水の硬度測定 硬度 キレート滴定 マスキング剤 Transblog




比色試薬 金属指示薬 Nn 同仁化学研究所




水道水と飲料水の硬度測定 硬度 キレート滴定 マスキング剤 Transblog



学生実験をみてみよう 第2期 その5 キレート滴定 江頭教授 東京工科大学 工学部 応用化学科 ブログ



キレート滴定の問題で Bt指示薬を使ってcaとmgの混合溶液のmgだけの濃度 Yahoo 知恵袋




容量分析法 キレート滴定 問題解説 Youtube
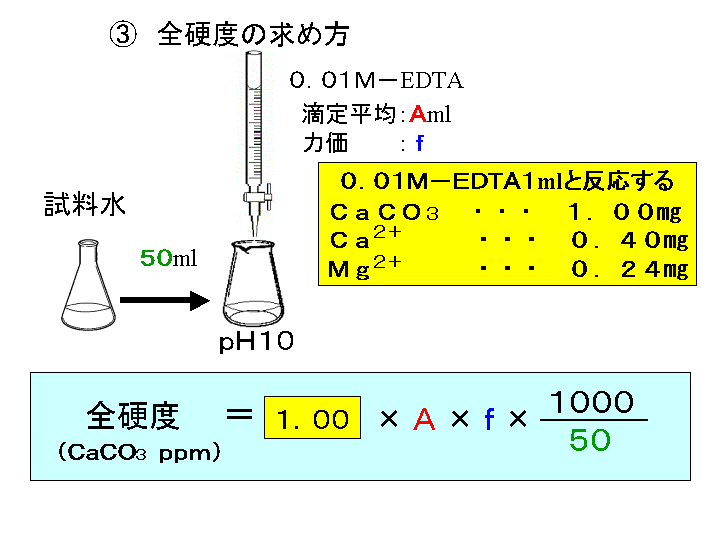



水の硬度測定 キレート滴定
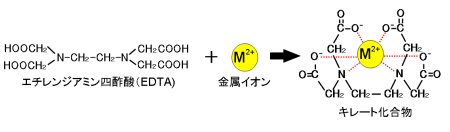



水の硬度測定 キレート滴定



0 件のコメント:
コメントを投稿